Autor:
Bobbie Johnson
Fecha De Creación:
10 Abril 2021
Fecha De Actualización:
1 Mes De Julio 2024
Contenido
- Pasos
- Parte 1 de 2: preparar el equipo
- Parte 2 de 2: Realizar un experimento
- Consejos
- Advertencias
- Qué necesitas
Proceso de división del agua (H2O) en sus componentes (hidrógeno y oxígeno) utilizando electricidad se llama electrólisis. Los gases obtenidos como resultado de la electrólisis se pueden utilizar por sí solos; por ejemplo, el hidrógeno sirve como una de las fuentes de energía más limpias. Si bien el nombre de este proceso puede parecer un poco inteligente, en realidad es más fácil de lo que parece si tiene el equipo, los conocimientos y un poco de experiencia adecuados.
Pasos
Parte 1 de 2: preparar el equipo
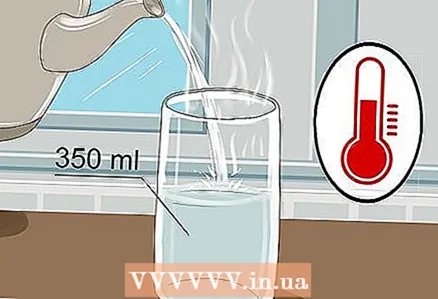 1 Tome un vaso de 350 ml y vierta agua tibia en él. No es necesario llenar el vaso hasta el borde, basta con un poco de agua. El agua fría servirá, aunque el agua caliente conduce mejor la electricidad.
1 Tome un vaso de 350 ml y vierta agua tibia en él. No es necesario llenar el vaso hasta el borde, basta con un poco de agua. El agua fría servirá, aunque el agua caliente conduce mejor la electricidad. - Tanto el agua del grifo como el agua embotellada servirán.
- El agua tibia tiene una viscosidad más baja, lo que facilita el movimiento de los iones.
 2 Disuelve 1 cucharada (20 gramos) de sal de mesa en agua. Vierta sal en un vaso y revuelva el agua para que se disuelva. Esto creará una solución salina.
2 Disuelve 1 cucharada (20 gramos) de sal de mesa en agua. Vierta sal en un vaso y revuelva el agua para que se disuelva. Esto creará una solución salina. - El cloruro de sodio (es decir, sal de mesa) es un electrolito que aumenta la conductividad eléctrica del agua. Por sí sola, el agua no conduce bien la electricidad.
- Después de aumentar la conductividad eléctrica del agua, la corriente creada por la batería pasará más fácilmente a través de la solución y descompondrá más eficazmente las moléculas en hidrógeno y oxígeno.
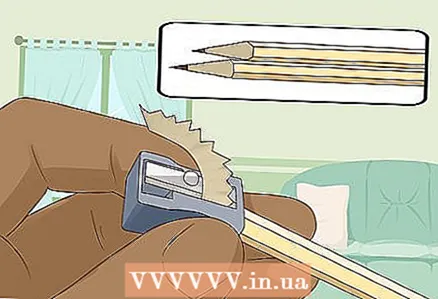 3 Afile dos lápices duros y blandos en ambos extremos para exponer la mina. No olvide quitar el borrador de sus lápices. Una varilla de grafito debe sobresalir en ambos extremos.
3 Afile dos lápices duros y blandos en ambos extremos para exponer la mina. No olvide quitar el borrador de sus lápices. Una varilla de grafito debe sobresalir en ambos extremos. - Las varillas de grafito servirán como electrodos aislados a los que se conecta la batería.
- El grafito es muy adecuado para este experimento porque no se disuelve ni se corroe en el agua.
 4 Recorta una hoja de cartón lo suficientemente grande como para colocarla encima del vaso. Use un trozo de cartón bastante grueso que no se doble después de perforar dos agujeros. Corta una pieza cuadrada de una caja de zapatos o similar.
4 Recorta una hoja de cartón lo suficientemente grande como para colocarla encima del vaso. Use un trozo de cartón bastante grueso que no se doble después de perforar dos agujeros. Corta una pieza cuadrada de una caja de zapatos o similar. - El cartón se usa para sostener los lápices en el agua para que no toquen los lados y el fondo del vaso.
- El cartón no es conductor, por lo que puede colocarlo de forma segura sobre un vaso.
 5 Usa lápices para hacer dos agujeros en el cartón. Perfore el cartón con lápices; en este caso, estarán bien sujetos y no se deslizarán. Asegúrese de que el grafito no toque los lados o el fondo del vidrio, de lo contrario interferirá con el experimento.
5 Usa lápices para hacer dos agujeros en el cartón. Perfore el cartón con lápices; en este caso, estarán bien sujetos y no se deslizarán. Asegúrese de que el grafito no toque los lados o el fondo del vidrio, de lo contrario interferirá con el experimento.
Parte 2 de 2: Realizar un experimento
 1 Conecte un cable con pinzas de cocodrilo a cada terminal de la batería. La batería servirá como fuente de corriente eléctrica, y a través de los cables con abrazaderas y varillas de grafito, la corriente llegará al agua.Conecte un cable con una abrazadera al positivo y el otro al terminal negativo de la batería.
1 Conecte un cable con pinzas de cocodrilo a cada terminal de la batería. La batería servirá como fuente de corriente eléctrica, y a través de los cables con abrazaderas y varillas de grafito, la corriente llegará al agua.Conecte un cable con una abrazadera al positivo y el otro al terminal negativo de la batería. - Utilice una batería de 6 voltios. Si no tiene una, puede usar una batería de 9 voltios.
- Se puede obtener una batería adecuada en una tienda de suministros eléctricos o en un supermercado.
 2 Conecte los otros extremos de los cables a los lápices. Fije las abrazaderas de alambre de metal firmemente a las varillas de grafito. Es posible que deba quitar un poco más de madera de los lápices para evitar que los clips se salgan de las varillas de grafito.
2 Conecte los otros extremos de los cables a los lápices. Fije las abrazaderas de alambre de metal firmemente a las varillas de grafito. Es posible que deba quitar un poco más de madera de los lápices para evitar que los clips se salgan de las varillas de grafito. - Por lo tanto, cerrará el circuito y la corriente de la batería fluirá a través del agua.
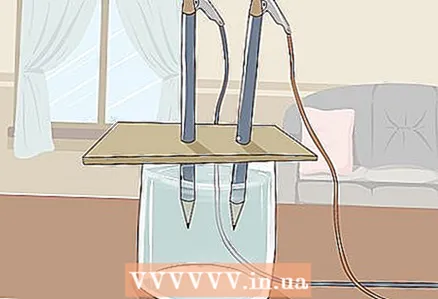 3 Coloca el cartón sobre el vaso de manera que los extremos libres de los lápices queden sumergidos en el agua. La hoja de cartón debe ser lo suficientemente grande para descansar sobre el vidrio. Tenga cuidado de no perturbar la correcta colocación de los lápices.
3 Coloca el cartón sobre el vaso de manera que los extremos libres de los lápices queden sumergidos en el agua. La hoja de cartón debe ser lo suficientemente grande para descansar sobre el vidrio. Tenga cuidado de no perturbar la correcta colocación de los lápices. - Para que el experimento tenga éxito, el grafito no debe tocar las paredes ni el fondo del vidrio. Verifique esto nuevamente y ajuste los lápices si es necesario.
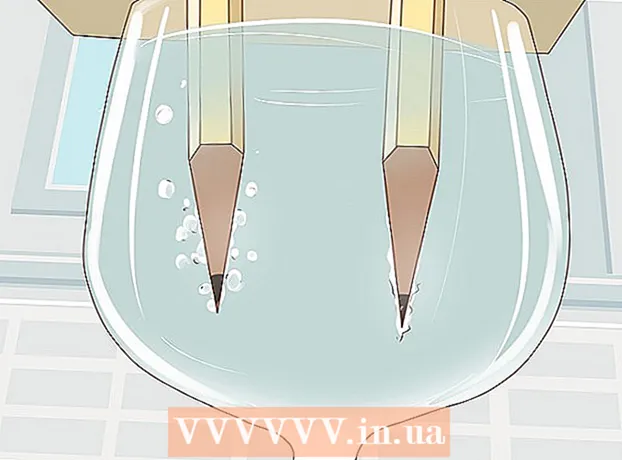
 4 Observa cómo el agua se divide en hidrógeno y oxígeno. Las burbujas de gas comenzarán a salir de las varillas de grafito sumergidas en el agua. Estos son hidrógeno y oxígeno. Se liberará hidrógeno en el polo negativo y oxígeno en el polo positivo.
4 Observa cómo el agua se divide en hidrógeno y oxígeno. Las burbujas de gas comenzarán a salir de las varillas de grafito sumergidas en el agua. Estos son hidrógeno y oxígeno. Se liberará hidrógeno en el polo negativo y oxígeno en el polo positivo. - Tan pronto como conecte los cables a la batería y las varillas de grafito, fluirá una corriente eléctrica a través del agua.
- Se formarán más burbujas de gas en el lápiz que está conectado al polo negativo, ya que cada molécula de agua está formada por dos átomos de hidrógeno y un átomo de oxígeno.
Consejos
- Si no tiene lápices con varillas de grafito, puede usar dos alambres pequeños en su lugar. Simplemente envuelva un extremo de cada cable alrededor del polo de la batería correspondiente y sumerja el otro en el agua. El resultado será el mismo que con los lápices.
- Intente usar una batería diferente. La cantidad de corriente que fluye depende del voltaje de la batería, lo que, a su vez, afecta la velocidad de división de las moléculas de agua.
Advertencias
- Si agrega un electrolito, como sal, al agua, tenga en cuenta que el experimento generará una pequeña cantidad de un subproducto como el cloro. Es seguro en cantidades tan pequeñas, pero puede oler un ligero olor a cloro.
- Realice este experimento bajo la supervisión de un adulto. Está asociado con la electricidad y los gases y, por lo tanto, puede ser peligroso, aunque poco probable.
Qué necesitas
- Dos lápices duros y blandos
- Una batería de 6 o 9 voltios
- Vidrio con un volumen de 350 mililitros.
- 2 hilos con pinzas de cocodrilo
- Sacapuntas para lápiz
- Sal



