Autor:
Frank Hunt
Fecha De Creación:
13 Marcha 2021
Fecha De Actualización:
1 Mes De Julio 2024

Contenido
- Al paso
- Método 1 de 3: uso de un medidor de pH
- Método 2 de 3: con papel tornasol
- Método 3 de 3: Comprensión del pH
Es importante medir el pH (el grado de acidez o alcalinidad) del agua. El agua es utilizada por las plantas y los animales de los que dependemos, y la bebemos todos los días. El valor del pH del agua puede ser una indicación de una posible contaminación, por lo que medir el pH del agua puede ser una importante precaución de salud pública.
Al paso
Método 1 de 3: uso de un medidor de pH
 Calibre la sonda y el medidor de acuerdo con las instrucciones de fábrica. Es posible que deba calibrar el medidor con una sustancia con un valor de pH conocido. El medidor se puede ajustar de acuerdo con esa sustancia. Si va a analizar el agua fuera de un laboratorio, se recomienda que realice esta calibración unas horas antes de la prueba de campo.
Calibre la sonda y el medidor de acuerdo con las instrucciones de fábrica. Es posible que deba calibrar el medidor con una sustancia con un valor de pH conocido. El medidor se puede ajustar de acuerdo con esa sustancia. Si va a analizar el agua fuera de un laboratorio, se recomienda que realice esta calibración unas horas antes de la prueba de campo. - Enjuague la sonda con agua limpia antes de usarla. Secar con un paño limpio.
 Tome una muestra de agua y viértala en un recipiente limpio.
Tome una muestra de agua y viértala en un recipiente limpio.- El agua debe ser lo suficientemente profunda para sumergir la punta del electrodo.
- Deje la muestra por un tiempo para permitir que la temperatura se estabilice.
- Mida la temperatura de la muestra con un termómetro.
 Ajuste el medidor con la temperatura de la muestra. La sensibilidad de la sonda se ve afectada por la temperatura del agua, por lo que la medición solo puede ser precisa si ingresa los datos de temperatura.
Ajuste el medidor con la temperatura de la muestra. La sensibilidad de la sonda se ve afectada por la temperatura del agua, por lo que la medición solo puede ser precisa si ingresa los datos de temperatura.  Coloque la sonda en la muestra. Espere a que el medidor alcance el equilibrio. El medidor está en un estado estable cuando la lectura es estable.
Coloque la sonda en la muestra. Espere a que el medidor alcance el equilibrio. El medidor está en un estado estable cuando la lectura es estable.  Lea la medición de pH de la muestra. El medidor de pH da el resultado en una escala de 0-14. Si el agua es pura, el valor es de alrededor de 7. Escriba sus hallazgos.
Lea la medición de pH de la muestra. El medidor de pH da el resultado en una escala de 0-14. Si el agua es pura, el valor es de alrededor de 7. Escriba sus hallazgos.
Método 2 de 3: con papel tornasol
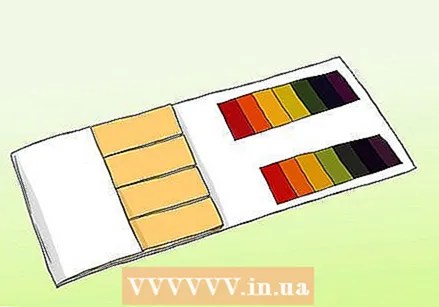 Aprenda la diferencia entre el papel de pH y el papel tornasol. Puede utilizar papel de pH para obtener una lectura precisa de una muestra. Sin embargo, el papel de pH no debe confundirse con el papel tornasol normal. Ambos pueden usarse para probar ácidos y bases, pero difieren en aspectos importantes.
Aprenda la diferencia entre el papel de pH y el papel tornasol. Puede utilizar papel de pH para obtener una lectura precisa de una muestra. Sin embargo, el papel de pH no debe confundirse con el papel tornasol normal. Ambos pueden usarse para probar ácidos y bases, pero difieren en aspectos importantes. - Las tiras de pH contienen una serie de barras indicadoras que cambian de color cuando se exponen a una solución. La fuerza de los ácidos y las bases en cada barra es diferente. Después del cambio, el patrón de color se puede comparar con las muestras suministradas con el kit.
- El papel tornasol es una tira de papel que contiene un ácido o una base (alcalina). Las rayas más comunes son rojas (con un ácido que reacciona con bases) y azules (con una base que reacciona con ácidos). Las rayas rojas se vuelven azules si la sustancia es alcalina y las rayas azules se vuelven rojas si la sustancia es ácida. Los papeles tornasol se pueden usar como una prueba rápida y fácil, pero las variedades más baratas no siempre dan una medida precisa de la fuerza de la solución.
 Tome una muestra del agua y viértala en un recipiente limpio. El agua debe ser lo suficientemente profunda para sumergir la tira.
Tome una muestra del agua y viértala en un recipiente limpio. El agua debe ser lo suficientemente profunda para sumergir la tira.  Sumerja una tira reactiva en la muestra. La exposición de unos segundos es suficiente. Las barras indicadoras del papel cambiarán de color después de unos momentos.
Sumerja una tira reactiva en la muestra. La exposición de unos segundos es suficiente. Las barras indicadoras del papel cambiarán de color después de unos momentos.  Compare el extremo de la tira reactiva con la tabla de colores que viene con el papel. El color o los colores de la tarjeta deben coincidir con el color o los colores de la tira reactiva. El mapa de color luego relaciona los patrones de color con los niveles de pH.
Compare el extremo de la tira reactiva con la tabla de colores que viene con el papel. El color o los colores de la tarjeta deben coincidir con el color o los colores de la tira reactiva. El mapa de color luego relaciona los patrones de color con los niveles de pH.
Método 3 de 3: Comprensión del pH
 Aprenda cómo se definen los ácidos y las bases. La acidez y la alcalinidad (el término utilizado para describir las bases) se definen por los iones de hidrógeno que donan o absorben. Un ácido es una sustancia que dona (o "dona") iones de hidrógeno y una base es una sustancia que absorbe iones de hidrógeno adicionales.
Aprenda cómo se definen los ácidos y las bases. La acidez y la alcalinidad (el término utilizado para describir las bases) se definen por los iones de hidrógeno que donan o absorben. Un ácido es una sustancia que dona (o "dona") iones de hidrógeno y una base es una sustancia que absorbe iones de hidrógeno adicionales.  Comprende la escala de pH. El número de pH se utiliza para medir el grado de acidez o alcalinidad de sustancias solubles en agua. El agua normalmente tiene la misma cantidad de iones hidróxido (OH-) e iones hidronio (H3O +). La proporción de iones hidróxido e hidronio cambia cuando se agrega una sustancia ácida o alcalina al agua.
Comprende la escala de pH. El número de pH se utiliza para medir el grado de acidez o alcalinidad de sustancias solubles en agua. El agua normalmente tiene la misma cantidad de iones hidróxido (OH-) e iones hidronio (H3O +). La proporción de iones hidróxido e hidronio cambia cuando se agrega una sustancia ácida o alcalina al agua. - Por lo general, se considera una escala que va de 0 a 14 (aunque las sustancias pueden quedar fuera de este rango). Las sustancias neutras puntúan alrededor de 7, las sustancias ácidas están por debajo de 7 y las sustancias alcalinas por encima de 7.
- La escala de pH es logarítmica, lo que significa que las diferencias enteras representan una diferencia de diez veces en acidez o alcalinidad. Por ejemplo, una sustancia con un pH de 2 es diez veces más ácida que una sustancia con un pH de 3 y 100 veces más ácida que una sustancia con un pH de 4. La escala funciona de la misma manera con las sustancias alcalinas, con cualquier el ser entero representa una diferencia de diez veces.
 Descubra por qué analizamos el pH del agua. El agua pura tiene un pH de 7, pero el agua del grifo holandesa suele tener un pH de entre 7,5 y 8,3. Es más probable que el agua muy ácida (agua con un valor de pH bajo) disuelva los productos químicos tóxicos. Estos pueden contaminar el agua y hacer que no sea seguro beberla.
Descubra por qué analizamos el pH del agua. El agua pura tiene un pH de 7, pero el agua del grifo holandesa suele tener un pH de entre 7,5 y 8,3. Es más probable que el agua muy ácida (agua con un valor de pH bajo) disuelva los productos químicos tóxicos. Estos pueden contaminar el agua y hacer que no sea seguro beberla. - En general, se recomienda probar el pH in situ. Si toma una muestra de agua para una investigación de laboratorio, el dióxido de carbono (CO2) del aire puede disolverse en el agua. El dióxido de carbono disuelto reacciona con los iones del agua y aumenta la acidez en soluciones básicas o neutras. Para evitar la contaminación por dióxido de carbono, el agua debe analizarse dentro de las dos horas posteriores a la recolección.